Менструальный цикл. Овуляция. Менструация (месячные)
Реализация нормального менструального цикла, который сопровождается возможным наступлением беременности, требует согласованности действий яичников и отделов головного мозга, отвечающих за функцию размножения и осуществляющих контроль над его качеством и безопасностью для матери и плода. Поэтому репродуктивная система по определению — функциональная система (П.К. Анохин, 1933). Она представляет собой построенную по иерархическому типу динамическую организацию структур и процессов организма, интегрирующую деятельность отдельных компонентов, независимо от их анатомической, тканевой и физиологической принадлежности, в направлении обеспечения процессов зачатия, вынашивания беременности, деторождения, вскармливания и воспитания потомства. Регуляция осуществляется по принципу обратной связи между центральными и периферическими звеньями. Поразителен тот факт, что репродуктивная система до наступления беременности истово защищает интересы материнского организма и в неблагоприятных для организма условиях предпочитает предотвратить наступление беременности. В то же время после её наступления главным становится обеспечение интересов плода, порой в ущерб материнскому организму, ввиду отсутствия реальных механизмов самооценки адаптации к наступившей беременности.
Менструальный цикл — одно из наиболее значимых проявлений сложных биологических процессов в организме женщины, характеризующихся циклическими изменениями функции репродуктивной, сердечно-сосудистой, нервной, эндокринной, иммунной и других систем организма, которые носят двухфазный характер, что связано с ростом и созреванием фолликула, овуляцией и развитием жёлтого тела в яичниках. Их биологическое значение состоит в подготовке, осуществлении и контроле над процессами созревания яйцеклетки, её оплодотворением и имплантацией зародыша в матке (рис. 6--18).
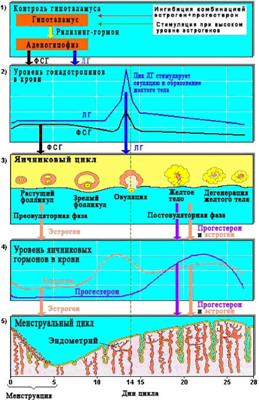
Рис. 6-18. Схема регуляции менструального цикла.
Наиболее выраженные циклические изменения происходят в эндометрии. В отсутствие имплантации функциональный слой его отторгается, и цикл заканчивается менструальным кровотечением. Длительность одного менструального цикла определяют от первого дня наступившей менструации до первого дня следующей менструации. В норме у здоровых женщин он составляет 21–35 дней, при этом у большинства женщин (55–60%) менструальный цикл длится 28–30 дней.
Существует пять уровней в иерархии репродуктивной системы: органы/тканимишени, яичники, передняя доля гипофиза, гипофизотропная зона гипоталамуса и надгипоталамические церебральные структуры.
Первый уровень составляют органы/тканимишени, которые отвечают на воздействие половых стероидов посредством их связи с расположенными в цито-плазме клеток специфическими рецепторами, количество и активность которых в зависимости от фазы менструального цикла изменяется в соответствии с динамикой концентрации половых гормонов в течение менструального цикла. Помимо наружных и внутренних половых органов, к ним относят молочные железы, ЦНС, кожу и её придатки, костную, мышечную и жировую ткань, а также слизистые оболочки мочевыводящих путей и толстой кишки. Кроме того, метаболизм клеток тканей-мишеней находится в зависимости от количества внутриклеточного цАМФ и межклеточных регуляторов — простагландинов (ПГ).
По характеру морфофункциональных циклических изменений в эндометрии различают фазы пролиферации, секреции, десквамации и регенерации (рис. 6--19).
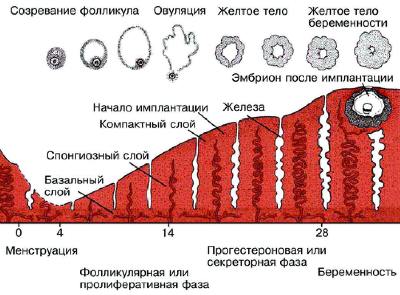
Рис. 6-19. Маточный и яичниковый циклы.
Фаза пролиферации (фолликулярная) при 28-дневном цикле продолжается в среднем 14 дней. Сразу после менструации под влиянием постепенно повышающейся концентрации эстрадиола происходят бурный рост и пролиферация функционального слоя эндометрия и желёз, которые удлиняются и разрастаются глубоко в подэпителиальном слое (строме). Спиральные артерии растут к поверхности от глубокого слоя эндометрия между удлиняющимися железами. Признак пролиферативного эндометрия — наличие митозов в эпителии. Непосредственно перед овуляцией железы эндометрия становятся максимально длинными, штопорообразно извитыми, спиральные артерии достигают поверхности эндометрия, становятся извитыми, сеть аргирофильных волокон концентрируется в строме вокруг желёз эндометрия и кровеносных сосудов. Толщина функционального слоя эндометрия к концу фазы пролиферации составляет 4–5 мм.
Фаза секреции (лютеиновая) при 28-дневном цикле в среднем также длится 14 дней и непосредственно связана с активностью жёлтого тела. Сразу после овуляции под влиянием постепенно повышающейся концентрации прогестерона эпителий желёз начинает вырабатывать секрет, содержащий кислые гликозаминогликаны, гликопротеиды и гликоген. Количество митозов в железистом эпителии уменьшается, и клетки формируют один цилиндрический слой внутри железы. Просвет желёз расширяется, в них появляются крупные субнуклеарные вакуоли, содержащие гликоген и липиды.
В средней стадии фазы секреции (19–23--й дни), когда наряду с максимальной концентрацией прогестерона наблюдают повышение содержания эстрогенов, функциональный слой эндометрия становится более высоким, достигая 8–10 мм, и отчётливо разделяется на два слоя. Глубокий (губчатый, спонгиозный) слой граничит с базальным, он содержит большое количество желёз и небольшое — стромы. Плотный (компактный) слой составляет 20–25% толщины функционального слоя, в нём содержится меньше желёз и больше клеток соединительной ткани. В просвете желёз находится секрет, содержащий гликоген и кислые мукополисахариды. Наивысшую степень секреции наблюдают на 20–21-й день менструального цикла. К этому моменту в эндометрии накапливается максимальное количество протеолитических и фибринолитических ферментов. В строме возникают децидуальноподобные превращения — клетки компактного слоя становятся крупными, приобретая округлую или полигональную форму, характерный «пенистый вид», в их цитоплазме появляется гликоген. Спиральные артерии резко извиты, образуют «клубки» и обнаруживаются во всём функциональном слое. Вены расширены. В средней стадии фазы секреции происходит имплантация бластоцисты, наиболее благоприятный для этого период — 20–22--й дни (6–8--й дни после овуляции). Поздняя стадия фазы секреции (24–27--й дни) в связи с началом регресса жёлтого тела и снижением концентрации продуцируемых им гормонов характеризуется нарушением трофики эндометрия и постепенным нарастанием в нём дегенеративных изменений. Уменьшается высота эндометрия (на 20–30% по сравнению со средней фазой секреции), строма функционального слоя сморщивается, усиливается складчатость стенок желёз, они приобретают звёздчатые или пилообразные очертания. Из зернистых клеток стромы эндометрия выделяются гранулы, содержащие релаксин, способствующий расплавлению аргирофильных волокон функционального слоя. На 26–27--й день цикла в поверхностных слоях компактного слоя наблюдают лакунарное расширение капилляров и очаговые кровоизлияния в строму. Состояние эндометрия, подготовленного таким образом к распаду и отторжению, называется анатомической менструацией и обнаруживается за сутки до начала клинической менструации.
В связи с регрессией и гибелью жёлтого тела, что влечёт за собой резкий спад концентрации гормонов, в эндометрии нарастают гипоксия и дегенеративные изменения. Длительный спазм артерий приводит к развитию стаза крови, образованию тромбов, повышению проницаемости и ломкости сосудов, кровоизлияниям в строму, лейкоцитарной инфильтрации. Развиваются некробиоз ткани и её расплавление. Вслед за длительным спазмом сосудов наступает их паретическое расширение, сопровождающееся усиленным притоком крови и разрывом стенки сосудов. Происходит отторжение (десквамация) некротизированных отделов функционального слоя эндометрия, которое обычно заканчивается на 3--й день цикла. Фаза десквамации немедленно сменяется регенерацией слизистой оболочки из тканей базального слоя (краевых отделов желёз). В физиологических условиях на 4--й день цикла вся раневая поверхность эндометрия эпителизируется.
Во время беременности строма эндометрия — важный источник некоторых пептидов, особенно пролактина, соматомедина С (фактора, связывающего инсулиноподобный фактор роста) и пептида, подобного паратгормону.
Второй уровень — яичники, в которых непрерывно, начиная с внутриутробного периода и заканчивая глубокой старостью женщины, происходят рост и созревание фолликулов (фолликулогенез), а также взаимосвязанный с этим процессом синтез стероидов (стероидогенез). Фолликулогенез (рис. 6--20) подразумевает собой цикл развития фолликула от примордиального до предовуляторного, с последующей овуляцией и образованием жёлтого тела.
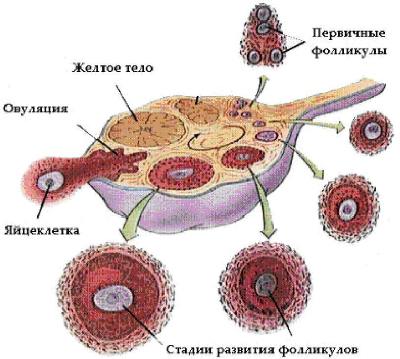
Рис. 6-20. Схема развития фолликула.
У взрослой женщины ежемесячно созревают примерно 20 фолликулов, что биологически необходимо для быстрой регенерации эндометрия под воздействием суммарного количества синтезируемых ими эстрогенов. Однако, поскольку для человека типична беременность одним плодом, на протяжении менструального цикла овулирует только один фолликул, который получает наиболее адекватное кровоснабжение и имеет оптимальную чувствительность к рецепторам гонадотропинов. Это позволяет ему получить самую высокую митотическую активность, накопить максимальное количество фолликулостимулирующего гормона (ФСГ) в фолликулярной жидкости и осуществить самый интенсивный синтез эстрадиола и ингибина по сравнению со всеми другими растущими фолликулами. В результате они претерпевают атретические изменения на различных этапах созревания, а лидирующий фолликул становится доминантным и проходит полный цикл развития. Его размер к моменту овуляции в результате увеличения количества клеток гранулёзы с 0,5´106 до 50´106 возрастает с 2 мм (примордиальный фолликул) до 20–22 мм, объём фолликулярной жидкости соответственно увеличивается в 100 раз.
Примордиальный фолликул состоит из яйцеклетки, окружённой одним рядом уплощённых клеток эпителия, выстилающих фолликул изнутри. В процессе созревания фолликула яйцеклетка увеличивается, клетки фолликулярного эпителия размножаются и округляются, образуется зернистый слой фолликула (strarum granulosum).
В гранулёзных клетках зреющего фолликула есть рецепторы к гонадотропинам, регулирующим процессы фолликуло и стероидогенеза. В толще зернистой оболочки в результате секреции и распада клеток фолликулярного эпителия и транссудата из кровеносных сосудов появляется жидкость. Яйцеклетка оттесняется жидкостью к периферии, окружается 17–50 рядами клеток гранулёзы. Возникает яйценосный холмик (cumulus oophorus). Строма вокруг зреющего фолликула дифференцируется на наружное (tunica externa thecae folliculi) и внутреннее покрытие фолликула (tunica interna thecae folliculi). Когда фолликулярная жидкость начинает полностью окружать ооцит, зреющий фолликул превращается в зрелый (граафов пузырёк).
В фолликулярной жидкости резко увеличивается содержание эстрадиола и ФСГ. Пропорциональный подъём концентрации E2 в периферической крови включает механизм обратной связи и стимулирует выброс лютеинизирующего гормона (ЛГ) и разрыв стенки фолликула ЛГ (овуляцию) в предварительно подготовленной области (стигме). Изменения в стенке фолликула (истончение и потенциальная возможность разрыва) обеспечиваются повышением активности фермента коллагеназы и протеолитических ферментов фолликулярной жидкости, а также ПГ-F2a и ПГ-E2, окситоцина и релаксина. На месте разорвавшегося фолликула образуется жёлтое тело, клетки которого секретируют прогестерон, эстрадиол и андрогены. Полноценное жёлтое тело образуется только тогда, когда в предовуляторном фолликуле содержится достаточное количество гранулёзных клеток с высоким содержанием рецепторов к ЛГ.
Стероидные гормоны продуцируются клетками гранулёзы, клетками thecae folliculi interna и, в меньшей степени, theca folliculi externa. Клетки гранулёзы и тека-клетки преимущественно участвуют в синтезе эстрогенов и прогестерона, а клетки theca folliculi externa — в синтезе андрогенов. Исходный материал для всех стероидных гормонов — холестерол, образующийся из ацетата или липопротеидов низкой плотности, который поступает в яичник с током крови. Андрогены синтезируются в тека-клетках под влиянием ЛГ и с током крови попадают в гранулёзные клетки.
Конечные этапы синтеза (превращение андрогенов в эстрогены) происходят под влиянием ферментов ароматаз, образующихся при участии ФСГ.
В клетках гранулёзы образуется белковый гормон — ингибин, тормозящий выделение ФСГ. В фолликулярной жидкости, жёлтом теле, матке и маточных трубах обнаружен окситоцин, который секретируется яичником и оказывает лютеолитическое действие, способствуя регрессу жёлтого тела. Вне беременности в клетках гранулёзы и жёлтого тела в очень небольших количествах вырабатывается релаксин, в жёлтом теле беременности его содержание возрастает во много раз. Релаксин оказывает токолитическое действие на матку и способствует овуляции.
Третий уровень — передняя доля гипофиза (аденогипофиз). Здесь секретируются гормоны, тропные для
эндокринных желёз:
· гонадотропины (ФСГ, ЛГ, пролактин);
· тиреотропный гормон (ТТГ);
· соматотропный гормон;
· адренокортикотропный гормон (АКТГ);
· меланоцитстимулирующий гормон.
ФСГ и ЛГ — гликопротеиды, пролактин — полипептид. Железамишень для ФСГ и ЛГ — яичник, синхронный выброс ЛГ и ФСГ способ-ствует овуляции. ФСГ стимулирует рост фолликула, пролиферацию клеток гранулёзы, образование рецепторов ЛГ на поверхности клеток гранулёзы. ЛГ увеличивает образование андрогенов в тека-клетках и синтез прогестерона в лютеинизированных клетках гранулёзы после овуляции. Основная роль ПРЛ — стимуляция роста молочных желёз и регуляция лактации. Он оказывает гипотензивное действие, даёт жиромобилизующий эффект, контролирует деятельность жёлтого тела. Повышение уровня ПРЛ тормозит фолликулогенез и стероидогенез в яичниках.
Четвёртый уровень репродуктивной системы — гипофизотропная зона гипоталамуса (рис. 6--21), её вентромедиальные, дорсомедиальные и аркуатные ядра, обладающие нейросекреторной активностью — способностью синтезировать либерины и статины (рилизинг-гормоны).
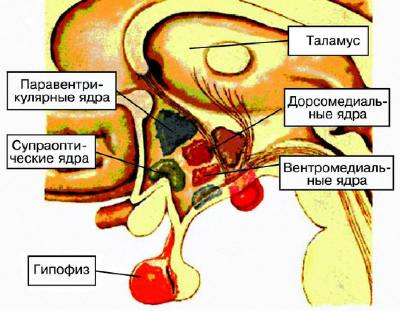
Рис. 6-21. Гипофизотропная зона гипоталамуса.
Выделен, синтезирован и описан ГнРГ (люлиберин), который стимулирует выделение клетками передней доли гипофиза ЛГ и, частично, ФСГ. ГнРГ из аркуатных ядер по аксонам нервных клеток попадает в терминальные окончания, тесно соприкасающиеся с капиллярами медиальной возвышенности гипоталамуса, которые формируют портальную кровеносную систему, объединяющую гипофиз и гипоталамус. Её особенность — возможность тока крови в обе стороны, что важно для осуществления механизма обратной связи.
Нейросекрет гипоталамуса оказывает биологическое воздействие на организм различными путями. Основной путь — парагипофизарный — через вены, впадающие в синусы твёрдой мозговой оболочки, а оттуда в ток крови.
Трансгипофизарный путь — через систему воротной вены к передней доле гипофиза. Обратное влияние на гипоталамус половых стероидов осуществляется через вертебральные артерии. Секреция ГнРГ генетически запрограммирована и происходит в определённом пульсирующем ритме с частотой примерно один раз в час. Этот ритм получил название цирхорального (часового). Он формируется в пубертатном возрасте и считается показателем зрелости нейросекреторных структур гипоталамуса. Цирхоральная секреция ГнРГ запускает гипоталамо-гипофизарно- яичниковую систему. Под влиянием ГнРГ происходит выделение ЛГ и ФСГ из клеток передней доли гипофиза. В модуляции пульсации ГнРГ играет роль эстрадиол. Величина выбросов ГнРГ в предовуляторный период (на фоне максимального выделения эстрадиола) значительно выше, чем в раннюю фолликулиновую и лютеиновую фазы.
Частота выбросов остаётся прежней. В дофаминергических нейронах аркуатного ядра гипоталамуса есть рецепторы к эстрадиолу.
Основная роль в регуляции выделения пролактина принадлежит дофаминергическим структурам гипоталамуса.
Дофамин тормозит выделение пролактина из гипофиза.
Пятый уровень регуляции менструального цикла — надгипоталамические церебральные структуры. Воспринимая импульсы из внешней среды и от интерорецепторов, они передают их через систему передатчиков нервных импульсов (нейротрансмиттеров) в нейросекреторные ядра гипоталамуса.
В эксперименте показано, что в регуляции функции гипоталамических нейронов, секретирующих ГнРГ, ведущая роль принадлежит дофамину, норадреналину и серотонину. Функцию нейротрансмиттеров выполняют нейропептиды морфиноподобного действия (опиоидные пептиды) — эндорфины и энкефалины, регулирующие функцию гипофиза.
Эндорфины подавляют секрецию ЛГ, а их антагонист — налоксон — приводит к резкому повышению секреции ГнРГ.
Считают, что эффект опиоидов осуществляется в результате изменения содержания дофамина (эндорфины снижают его синтез, вследствие чего стимулируются секреция и выделение пролактина).
В регуляции менструального цикла участвует кора большого мозга. Существуют данные об участии амигдалоидных ядер и лимбической системы в нейрогуморальной регуляции менструального цикла. Электрическое раздражение амигдалоидного ядра (в толще больших полушарий) вызывает в эксперименте овуляцию. Нарушения овуляции наблюдают при стрессовых ситуациях, перемене климата, ритма работы. Нарушения менструального цикла реализуются через изменение синтеза и потребления нейротрансмиттеров в нейронах мозга.
Таким образом, репродуктивная система представляет собой суперсистему, функциональное состояние которой определяется обратной связью входящих в неё подсистем, как отрицательной, так и положительной (овуляция).
Регуляция внутри этой системы может идти:
· по длинной петле обратной связи (гормоны яичника®ядра гипоталамуса; гормоны яичника®гипофиз);
· по короткой петле (передняя доля гипофиза®гипоталамус);
· по ультракороткой петле (ГнРГ®нервные клетки гипоталамуса).
Помимо изменений в системе «гипоталамус–гипофиз–яичники» и в органахмишенях на протяжении менструального цикла происходят изменения функционального состояния многих систем организма, которые у здоровой женщины находятся в пределах физиологических границ.
В ЦНС во время менструаций обнаружена некоторая тенденция к преобладанию тормозных реакций, снижению силы двигательных реакций. В фазе пролиферации отмечают преобладание тонуса парасимпатического отдела вегетативной нервной системы, в то время как в секреторной фазе — симпатического. Состояние сердечно- сосудистой системы в течение менструального цикла характеризуется волнообразными функциональными колебаниями. В 1-й фазе цикла капилляры несколько сужены, тонус всех сосудов повышен, ток крови быстрый, во 2-й фазе — капилляры несколько расширены, тонус сосудов снижен, ток крови не всегда равномерный.
Показатели гемоглобина (Hb) и количества эритроцитов наиболее высоки в первый день менструального цикла. Самое низкое содержание Hb отмечают на 24-й день цикла, а эритроцитов — ко времени овуляции. На протяжении менструального цикла меняется концентрация микроэлементов, азота, натрия, жидкости. Известны колебания настроения и нарушения когнитивных функций у женщин в предменструальном периоде.

