Токсоплазмоз — зоонозное протозойное заболевание, характеризующееся хроническим течением, полиморфизмом клинических проявлений, преимущественным поражением ЦНС, органов зрения, печени и лёгких.
Коды по МКБ -10
B58. Токсоплазмоз.
Включено: инфекция, вызванная Toxoplasma gondii.
Исключено: врождённый токсоплазмоз (P37.1).
B58.0. Токсоплазмозная окулопатия.
B58.1. Токсоплазмозный гепатит (K77.0).
B58.2. Токсоплазмозный менингоэнцефалит (G05.2).
B58.3. Лёгочный токсоплазмоз (J17.3).
B58.8. Токсоплазмоз с поражением других органов.
B58.9. Токсоплазмоз неуточнённый.
Причины, этиология токсоплазмоза
Возбудитель — Toxoplasma gondii (подцарство Protozoa, тип Apicomplecxa, отряд Coccidia, подотряд Eimeriina, семейство Eimeriidae).
В организме человека и животных T. gondii проходит несколько стадий развития: трофозоита (эндозоит, тахизоит), цисты (цистозоит, брадизоит) и ооцисты.
Трофозоиты размером 4–7×2–4 мкм напоминают по форме полумесяц. Цисты покрыты плотной оболочкой, размером до 100 мкм. Ооцисты овальной формы, диаметром 10–12 мкм.
По данным генотипирования различают три группы штаммов токсоплазм. Представители первой группы вызывают врождённый токсоплазмоз у животных.
У человека выявляют штаммы второй и третьей групп токсоплазм, причём представителей последней группы чаще обнаруживают у больных ВИЧ-инфекцией.
Определена антигенная структура различных стадий развития токсоплазм и установлено, что трофозоиты и цисты имеют как общие, так и характерные только для каждой из них антигены.
T. gondii — облигатный внутриклеточный паразит, внедряющийся в эпителиальные клетки кишки и размножающийся в них посредством эндодиогении. Затем трофозоиты (тахизоиты) с током крови и лимфы попадают в другие органы и ткани (лимфатические узлы, печень, лёгкие и др.), где активно проникают в клетки. В поражённых клетках возникают скопления эндозоитов одной генерации, окружённые мембраной паразитофорной вакуоли (так называемые псевдоцисты).
В результате ответной иммунной реакции хозяина паразиты исчезают из крови и в инфицированных клетках-мишенях формируются покрытые плотной оболочкой цисты. При хроническом течении заболевания T. gondii в виде расположенных внутриклеточно цист сохраняют жизнеспособность неопредёленно долго. Цисты локализуются преимущественно в головном мозге, сердечной и скелетных мышцах, матке, глазах.
Основные хозяева T. gondii — представители семейства Felidae (кошачьи) одновременно могут быть и промежуточными хозяевами, поскольку в их организме токсоплазмы способны перемещаться из кишки в клетки различных органов. Посредством мерогонии паразит размножается в эпителиальных клетках кишки; в результате образуются мерозоиты. Часть из них даёт начало мужским и женским половым клеткам — гамонтам. После выхода из энтероцитов мужские гамонты многократно делятся, образуя микрогаметы («сперматозоиды»); из женских гамонтов формируются макрогаметы («яйцеклетки»). После оплодотворения формируется незрелая ооциста, которая с фекальными массами выводится в окружающую среду. При благоприятных условиях созревание ооцист (спорогония) продолжается от 2 сут до 3 нед. Зрелые цисты устойчивы к действию неблагоприятных факторов внешней среды и могут сохранять жизнеспособность до года и дольше.
Эпидемиология токсоплазмоза
Окончательные хозяева паразита — домашняя кошка и другие представители семейства кошачьих (рысь, пума, ягуар и др.). Промежуточные хозяева — различные виды грызунов, хищных сумчатых, насекомоядных, непарно- и парнокопытных, приматов, зайцеобразных и птиц, человек. Основное значение в распространении заболевания имеют кошки, которые в свою очередь заражаются, поедая грызунов, птиц, мясо домашних животных и проглатывая ооцисты. У животных возможен также трансплацентарный путь передачи возбудителя. Человек заражается пероральным путём при употреблении мяса, содержащего тканевые цисты (сырое или недостаточно термически обработанное); попадании ооцист из окружающей среды (с продуктами или водой, при несоблюдении правил личной гигиены). Возможно заражение через повреждённую кожу и слизистые оболочки при тесном контакте с контаминированным животным сырьём (у работников мясокомбинатов, скотобоен и др.). Описаны случаи инфицирования при пересадке органов. Источник возбудителя для плода — только беременная с приобретённым токсоплазмозом. Передача возбудителя начинается с 3-го месяца беременности и достигает максимума в III триместре. У женщин, родивших инфицированного ребёнка, при последующих беременностях возбудитель плоду не передаётся.
Иммунитет при токсоплазмозе нестерильный, однако довольно напряжённый, и реинвазии не происходит. В большинстве случаев у людей без патологий иммунной системы результат заражения T. gondii — формирование здорового носительства.
Возбудитель встречается повсеместно. Степень инвазированности населения в разных странах колеблется в широких пределах (от 5–10 до 50% и больше); зависит от санитарно-гигиенических условий и особенностей питания населения.
В развивающихся странах токсоплазмозом чаще заражается детское население, в развитых странах этот показатель выше у взрослых.
Патогенез токсоплазмоза
Из места внедрения (чаще всего — полые органы пищеварения) токсоплазмы с током лимфы попадают в регионарные лимфатические узлы, где они размножаются и вызывают развитие лимфаденита. Затем паразиты в большом количестве поступают в кровь и разносятся по всему организму, вследствие чего возникают очаги поражения в нервной системе, печени, селезёнке, лимфатических узлах, скелетных мышцах, миокарде, глазах. Вследствие размножения трофозоитов разрушаются заражённые клетки. Вокруг очагов некроза и скопления токсоплазм формируются специфические гранулёмы. При нормальном иммунном ответе организма трофозоиты исчезают из тканей и начинается процесс формирования цист (воспалительная реакция вокруг них слабая). Заболевание переходит из острой фазы в хроническую, а ещё чаще — в хроническое носительство с сохранением цист в тканях органов. В неблагоприятных для организма условиях (острые заболевания и стрессовые ситуации, оказывающие иммуносупрессивное воздействие) оболочки цист разрушаются; высвободившиеся паразиты, размножаясь, поражают интактные клетки и поступают в кровоток, что клинически проявляется обострением хронического токсоплазмоза. Воспалительные инфильтраты и некрозы обнаруживают в скелетных мышцах, миокарде, лёгких и других органах. В головном мозге появляются воспалительные очаги с последующим некрозом, что иногда приводит к образованию петрификатов. В сетчатке и сосудистой оболочке глаза возникает продуктивно-некротическое воспаление. Злокачественное течение токсоплазмоз приобретает на фоне развёрнутой картины СПИДа, при этом развивается генерализованная форма заболевания, в ряде случаев являющаяся причиной гибели больных.
В ответ на антигены токсоплазм вырабатываются специфические антитела и развивается иммунная реакция по типу ГЗТ.
При врождённом токсоплазмозе в результате паразитемии возбудитель заносится в плаценту, формируя первичный очаг, а из него с током крови попадает в плод.
Он заражается независимо от наличия клинических проявлений у беременной, но исход зависит от того, в каком сроке беременности произошло инфицирование.
Заражение на ранних сроках эмбриогенеза заканчивается спонтанным выкидышем, мертворождением, вызывает тяжёлые, часто несовместимые с жизнью нарушения развития (анэнцефалии, анофтальмии и др.) или приводит к развитию генерализованного токсоплазмоза. При заражении в III триместре беременности преобладают асимптоматические формы течения, поздние клинические признаки которых проявляются через месяцы и годы.
Симптомы (клиническая картина) токсоплазмоза
Инкубационный период длится от нескольких недель до нескольких месяцев.
В зависимости от механизма заражения выделяют приобретённый и врождённый токсоплазмоз.
Приобретённый токсоплазмоз
Протекает обычно бессимптомно (до 99% всех случаев заражения T. gondii). Это здоровые люди, обычно с низким уровнем антитоксоплазменных антител, не нуждающиеся ни в медицинском наблюдении, ни в лечении. У лиц с нормальным иммунным ответом в большинстве случаев токсоплазмоз протекает в латентной форме. Манифестный токсоплазмоз протекает в острой (до 0,01% инфицированных) и хронической (1–5%) форме, имея склонность к рецидивам и обострениям.
Острая форма. У лиц с нормальным иммунным ответом заболевание часто клинически не проявляется. О заражении свидетельствует наличие у них в крови специфических IgМ-антител с повышением их уровня в динамике и последующей сменой на IgG. При развитии манифестной формы острого приобретённого токсоплазмоза инкубационный период длится от нескольких дней до недель.
Заболевание проявляется лихорадкой, синдромом интоксикации, лимфоаденопатией, лимфоцитозом; возникают высыпания на коже, диарея. Поражение скелетных мышц проявляется миалгией, часто возникают боли в суставах. Выражены гепатолиенальный синдром и признаки поражения ЦНС. Возможны катаральные проявления, пневмония, миокардит.
Хроническая форма приобретённого токсоплазмоза может развиться первично или вследствие перенесённой острой формы заболевания. В манифестных случаях хронический токсоплазмоз характеризуется полиморфизмом клинических проявлений. Начало постепенное, со слабовыраженных проявлений общего характера: головной боли, общей слабости, повышенной утомляемости, снижения памяти, неврозоподобных изменений, нарушения сна, держащейся длительное время субфебрильной температуры тела. У большинства больных выявляют лимфоаденопатию, миозиты, артралгии. При поражении миокарда больные предъявляют жалобы на одышку, сердцебиение, боли в области сердца. ЭКГ-данные свидетельствуют о развитии миокардита или миокардиодистрофии. Возможны интерстициальные пневмонии, хронический гастрит, энтероколит, поражения желчевыводящих путей и женской половой системы (нарушения менструального цикла, сальпингоофорит, эндометрит, бесплодие).
Важную роль при приобретённом хроническом токсоплазмозе играет поражение нервной системы: головного мозга, его оболочек, гипоталамуса, периферических нервов. Выявляют менингоэнцефалит, энцефалит, церебральный арахноидит, диэнцефальные и психические расстройства, судорожный синдром.
При поражении глаз возможны патологические изменения во всех оболочках, возникают поражения зрительного нерва, наружных мышц глазного яблока. В сочетании с хориоретинитом и другими изменениями иногда отмечают кератосклерит или кератоувеит.
У лиц с иммунодефицитным состоянием (например, СПИД, злокачественные лимфомы, состояния вследствие применения иммунодепрессантов) латентное течение токсоплазмоза или новое заражение, как и при других оппортунистических инфекциях, переходит в генерализованный процесс с поражением головного мозга, миокарда, лёгких и других тканей и органов. Активация латентного токсоплазмоза у ВИЧ-инфицированных происходит при содержании CD4+-лимфоцитов меньше 0,1×109 клеток в литре крови. При этом диссеминированный процесс развивается у 25–50% больных, имеющих специфические антитела. Чаще всего поражается ЦНС — развивается тяжёлый некротический энцефалит. Церебральный токсоплазмоз выявляют в разных странах у 3–40% больных СПИДом. В клинической картине преобладают симптомы очагового энцефалита, свидетельствующие о поражении полушарий головного мозга, мозжечка или ствола мозга (гемипарез, афазия, дезориентация, гемианопсия, судорожный синдром и другие изменения) и часто сочетающиеся с энцефалопатией. Внемозговую локализацию токсоплазмоза при СПИДе выявляют в 1,5–2% случаев, чаще всего в виде поражения глаз (50%), проявляющегося очаговым некротизирующим хориоретинитом без воспалительной реакции, однако могут вовлекаться и другие органы (сердце, лимфатические узлы, костный мозг, печень, поджелудочная железа, мочеполовая система и др.). Поражение лёгких возникает в 2% случаев.
У детей с ВИЧ-инфекцией заболевание протекает в латентной форме. Среди клинических форм чаще выявляют церебральную, глазную, лёгочную, миокардитическую, лимфонодулярную, а также поражение органов пищеварения.
Врождённый токсоплазмоз
Возникает только при инфицировании женщины в период беременности. У женщин с ВИЧ-инфекцией латентная, возникшая до беременности инвазия может реактивироваться. Врождённый токсоплазмоз в 25–30% случаев протекает с клиническими проявлениями, в остальных случаях — латентно. В зависимости от сроков инфицирования матери во время беременности врождённый токсоплазмоз у ребёнка может выражаться в различных формах.
Острая форма развивается при инфицировании на поздних сроках беременности. Она протекает как тяжёлое генерализованное заболевание с выраженной интоксикацией, лихорадкой, высыпаниями на коже, изъязвлениями на слизистой оболочке носоглотки, желтухой, отёками, гепатоспленомегалией. Позже возникает токсоплазмозный энцефалит. Выявляют поражение глаз и других органов.
Если ребёнок переносит острую форму внутриутробно, он может родиться с признаками хронического врождённого токсоплазмоза: с последствиями энцефалита в виде гидроцефалии, олигофрении, судорожного синдрома, с поражением глаз (вплоть до микро- и анофтальмии). Постепенно процесс переходит во вторично-хроническую форму с резидуальными явлениями.
При хроническом врождённом токсоплазмозе (резидуальные явления у детей и подростков) выявляют остаточные явления со стороны ЦНС и органов зрения: отставание в умственном и физическом развитии, гидроцефалию, микроцефалию, парезы и параличи, эпилептиформные припадки, микрофтальм, микрокорнеа, хориоретинит, атрофию зрительного нерва, катаракту, косоглазие, нистагм.
Диагностика
Клиническая диагностика
Диагноз ставят, выявляя эпидемиологические факторы риска инфицирования и учитывая данные клинической и лабораторной диагностики.
Специфическая и неспецифическая лабораторная диагностика
Паразитологические методы (иследование биоптатов лимфатических узлов и других органов) не находят широкого применения из-за их сложности и трудоёмкости. Специфические антитела классов IgM и IgG к антигенам токсоплазм выявляют в повторных серологических исследованиях: ИФА, РНГА и РИФ (но они недостаточно информативны у больных СПИДом); проводят внутрикожную пробу с токсоплазмином (нативным или рекомбинантным). При анализе и интерпретации результатов серологической диагностики следует учитывать «иммунологическую» инкубацию — появление антител на антигены паразита только через определённый латентный период — и оценивать результаты исследований в динамике. Кожная проба свидетельствует об инфицировании токсоплазмами, но не даёт информации о характере течения заболевания.
Беременным с положительными серологическими реакциями проводят УЗИ плода в динамике.
Инструментальные методы
При диагностике церебрального токсоплазмоза (особенно у больных СПИДом) проводят КТ, МРТ головного мозга; в сыворотке крови и СМЖ определяют титры IgG (реже IgM), выявляют ДНК возбудителя методом ПЦР и выделяют из них возбудитель.
Дифференциальная диагностика
Токсоплазмоз дифференцируют от многих заболеваний инфекционной и неинфекционной природы: лимфогранулематоза, лимфолейкоза и других патологий системы крови, туберкулёза, листериоза, иерсиниоза, инфекционного мононуклеоза, заболеваний нервной системы и органов зрения. У детей, с учётом возраста, токсоплазмоз необходимо дифференцировать от ЦМВИ, герпетических инфекций и различных ОРВИ, краснухи, вирусных гепатитов. При повторных выкидышах, рождении детей с аномалиями развития у серопозитивных женщин необходимо исключать акушерскую и гинекологическую патологию.
Лечение при токсоплазмозе
Наиболее эффективно в острой фазе заболевания; больные с латентной формой хронического приобретённого токсоплазмоза в лечении не нуждаются. Эффективность этиотропных ЛС при хроническом токсоплазмозе низкая, поскольку химиопрепараты и антибиотики практически не воздействуют на эндозоиты, находящиеся в тканевых цистах. При хроническом токсоплазмозе лечение показано только при обострении процесса и при невынашивании беременности (лечение проводят вне периода беременности).
В качестве этиотропных ЛС при токсоплазмозе применяют пириметамин в сочетании с сульфаниламидами или антибиотиками. Длительность цикла лечения 7 сут. Обычно проводят 2–3 цикла с перерывами между ними в 10 сут. Суточные дозы пириметамина и сульфадиазина приведены в таблице; антибиотики назначают в обычных дозах. Возможно применение ко-тримоксазола по одной таблетке два раза в сутки в течение 10 сут. Проводят два цикла с интервалом в 10 сут. Одновременно назначают кальция фолинат по 2–10 мг в сутки или дрожжи пивные по 5–10 таблеток в сутки. Необходимы контроль гемограммы (возможно угнетение костномозгового кроветворения) и общий анализ мочи в динамике.
Схема лечения приобретённого токсоплазмоза.
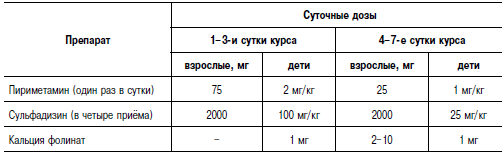
Беременных лечат спирамицином (накапливается в плаценте и не проникает в плод). Его назначают по 3 млн ЕД три раза в сутки в течение 2–3 нед. Лечение детей с врождённым токсоплазмозом проводят теми же препаратами, что и лечение взрослых: пириметамин по 1 мг/кг в сутки в два приёма в комбинации с сульфаниламидами короткого действия по 0,1 г/кг в сутки в 3–4 приёма.
Лечение проводят циклами: 5 сут принимают пириметамин, а сульфаниламидный препарат на 2 сут дольше — 7 сут. Проводят три цикла с перерывами между ними в 7–14 сут. Дополнительно назначают кальция фолинат по 1–5 мг один раз в 3 сут в течение всего курса лечения для устранения побочного действия антифолатов (пириметамина, сульфаниламидов). Такой же курс лечения по показаниям (например, хроническая форма заболевания, иммунодефицитное состояние, обострение хориоретинита) повторяют через 1–2 мес.
На втором месте по эффективности стоят макролиды, обладающие меньшей токсичностью. Спирамицин назначают по 150 000 ЕД/кг в сутки в 2 приёма в течение 10 сут, рокситромицин — по 5–8 мг/кг в сутки, азитромицин — по 5 мг/кг в сутки в течение 7–10 сут. При обострении хронического токсоплазмоза обычно достаточно одного курса этиотропного лечения в течение 7–10 сут.
Патогенетическое лечение проводят в зависимости от характера органной патологии. При необходимости назначают иммунокорригирующие препараты, витамины, десенсибилизирующие ЛС.
Больным токсоплазмозом с ВИЧ-инфекцией назначают те же препараты, что и другим пациентам: пириметамин — в первые сутки 200 мг в комбинации с сульфадиазином (по 1 г четыре раза в сутки), клиндамицином (по 0,6 г шесть раз в сутки) или спирамицином (по 3 млн ЕД три раза в сутки). Одновременно больные принимают кальция фолинат по 10–50 мг в сутки. Курс лечения не менее 4 нед, затем назначают вторичную профилактику для предупреждения рецидивов: пириметамин по 50 мг в сутки и сульфадиазин по 0,5 г четыре раза в сутки. В связи со сложностью диагностики и тяжестью течения церебрального токсоплазмоза лечение назначают даже при подозрении на заболевание. Улучшение в течение 2–4 нед лечения с большой долей вероятности указывает на наличие токсоплазмоза.
Эффективность этиотропного лечения токсоплазмоза оценивают по клиническим признакам: улучшению общего состояния больного, исчезновению лимфаденита; меньшей выраженности гепатолиенального синдрома, признаков энцефалита, поражения глаз; отсутствию рецидивов заболевания в течение 12 мес и более.
Результаты серологических исследований, оценивая эффективность этиотропного лечения, не используют, поскольку титры специфических антител не коррелируют с характером клинического течения заболевания.
Прогноз
Прогноз для приобретённого токсоплазмоза благоприятный, поскольку преобладает латентная форма без клинических проявлений. Септические формы, наблюдающиеся у больных СПИДом и у пациентов с иммунодефицитным состоянием другой этиологии, протекают тяжело и могут закончиться летальным исходом.
Диспансеризация
В диспансерном наблюдении нуждаются больные с острой формой приобретённого и рецидивирующим течением хронического токсоплазмоза, а также серопозитивные к антигенам токсоплазмы ВИЧ-инфицированные пациенты. Объём и сроки диспансерного наблюдения зависят от клинической формы токсоплазмоза и характера течения заболевания. При врождённом токсоплазмозе у детей в зависимости от резидуальных явлений вопрос о диспансеризации решают совместно с невропатологами, офтальмологами и другими врачами. Некоторые пациенты нуждаются в пожизненном диспансерном наблюдении (с поражением глаз при неэффективности этиотропного лечения, серопозитивные к антигенам токсоплазмы ВИЧ-инфицированные пациенты).
Профилактика токсоплазмоза
Специфические меры профилактики
Основные мероприятия по предупреждению врождённого токсоплазмоза — своевременное обследование женщин детородного возраста и беременных в женских консультациях. У ВИЧ-инфицированных пациентов проводят первичную и вторичную профилактику токсоплазмоза. Цель первичной профилактики — предупредить заражение T. gondii или развитие токсоплазменного энцефалита у лиц с латентно протекающей формой заболевания. У ВИЧ-инфицированных с положительной серологической реакцией на токсоплазмоз проводят химиопрофилактику этиотропными препаратами. Цель вторичной профилактики или поддерживающего лечения — предупредить рецидивы токсоплазменного энцефалита у больных СПИДом.
Неспецифические меры профилактики
Профилактика токсоплазмоза состоит в тщательной термической обработке мясных продуктов и молока; соблюдении правил личной гигиены, особенно в группах риска (ветеринары, работники мясокомбинатов, охотники и др.); предотвращении загрязнения детских песочниц экскрементами кошек.


Комментарии