СИНДРОМ ПОЛИКИСТОЗНЫХ ЯИЧНИКОВ
Синдром поликистозных яичников (СПКЯ) — это патология структуры и функции яичников, характеризующаяся овариальной гиперандрогенией с нарушением менструальной и генеративной функции.
СИНОНИМЫ СИНДРОМА ПОЛИКИСТОЗНЫХ ЯИЧНИКОВ
Болезнь поликистозных яичников, первичные поликистозные яичники, синдром Штейна–Левенталя, склерополикистозные яичники. В более раннем источнике (2007г.) БПКЯ и СПКЯ разделены как формы ПКЯ
КОД ПО МКБ-10 E28.2 Синдром поликистоза яичников.
ЭПИДЕМИОЛОГИЯ СИНДРОМА ПОЛИКИСТОЗНЫХ ЯИЧНИКОВ
Частота СПКЯ — примерно 11% среди женщин репродуктивного возраста, в структуре эндокринного бесплодия доходит до 70%, а у женщин с гирсутизмом СПКЯ выявляют в 65–70% наблюдений.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ СИНДРОМА ПОЛИКИСТОЗНЫХ ЯИЧНИКОВ
Этиопатогенез СПКЯ до конца не изучен, несмотря на большое число предложенных теорий. Вместе с тем большинство исследователей считают СПКЯ гетерогенным заболеванием, наследственно обусловленным, характеризующимся нарушением менструального цикла, хронической ановуляцией, гиперандрогенией, увеличением размеров яичников и особенностями их морфологической структуры: двусторонним увеличением размеров яичников в 2–6 раз, гиперплазией стромы и текаклеток, множеством кистозноатрезирующихся фолликулов диаметром 5–8 мм, утолщением капсулы яичников.
Кардинальный признак СПКЯ — овариальная гиперандрогения. Суммируя имеющиеся научные работы по этой проблеме, можно определить следующие механизмы патогенеза.
Нарушение гонадотропной функции. Эра синтеза и применения ГнРГ в 80е гг. дала не только возможность индукции овуляции, но и более углублённого изучения роли нарушений гонадотропной функции в патогенезе СПКЯ. Выдвинули гипотезу о первичном нарушении цирхорального ритма выделения ГнРГ с периода пубертата как причины возникновения СПКЯ, возможно, генетически обусловленной. Важную роль отводят средовым (стрессорным) факторам, нарушающим нейроэндокринный контроль в регуляции секреции ГнРГ, в результате чего увеличивается базальный уровень синтеза ЛГ и происходит относительное уменьшение продукции ФСГ. Известно, что период полового созревания критический в жизни девочки, на фоне которого генетические и средовые факторы способствуют манифестации различных нейроэндокринных синдромов.
В результате избыточной стимуляции ЛГ повышается продукция андрогенов в текаклетках, формируется кистозная атрезия фолликулов с гиперплазией текаклеток, стромы, не происходит селекции и развития доминантного фолликула. В результате относительного дефицита ФСГ, необходимого для синтеза цитохрома Р450, который активирует ферменты для метаболизма андрогенов в эстрогены, происходит накопление андрогенов и дефицит эстрадиола. По механизмам отрицательной обратной связи уменьшение уровня эстрадиола стимулирует синтез ЛГ, что является вторым фактором для повышения базального уровня ЛГ. Кроме того, эстрогены (в основном эстрон), синтезируемые внегонадно из тестостерона в большом количестве, повышают чувствительность клеток гипофиза к ГнРГ, что способствует хронической гиперсекреции ЛГ. Гиперпродукция андрогенов приводит к атрезии фолликулов, гиперплазии стромы текаклеток и белочной оболочки. Кроме того, повышенные концентрации андрогенов положительно коррелируют с уровнем ингибина В, который подавляет секрецию ФСГ.
С другой стороны, увеличение секреции ГнРГ может быть не первичным, а вторичным в ответ на гиперпродукцию андрогенов и уменьшение синтеза эстрадиола в яичниках. При этом овариальная гиперандрогения — это результат нарушения аутопаракринной регуляции роста и созревания фолликулов, а также дисрегуляции цитохрома Р450с17. Вследствие этих нарушений снижается синтез эстрадиола, что по механизму обратной связи стимулирует секрецию ГнРГ. Овариальную гиперандрогению отмечают у пациенток с нормальным уровнем гонадотропинов. При этом показана гиперреакция текаклеток поликистозных яичников на нормальные уровни ЛГ.
Инсулинорезистентность и гиперинсулинемия. Впервые о сочетании гиперандрогении и инсулинорезистентности при СПКЯ было сообщено в 1980 г., что способствовало развитию гипотезы о том, что ожирение и гиперинсулинемия должны играть основную роль в патогенезе СПКЯ у пациенток с инсулинорезистентностью. Однако гиперинсулинемию отмечают также и у пациенток с нормальной массой тела и СПКЯ. Следовательно, ожирение способствует, но не относится к основным факторам развития инсулинорезистентности при СПКЯ. Частота инсулинорезистентности составляет 35–60%. Патогенетические механизмы инсулинорезистентности до конца не известны, многофакторны и у подавляющего большинства пациенток с СПКЯ обусловлены не дефектом инсулинового рецептора, а нарушениями на рецепторном и пострецепторном уровне трансдукции инсулинового сигнала в клетку.
В норме инсулин связывается с трансмембранным инсулиновым рецептором, активируя несколько процессов, в частности аутофосфорилирование тирозина и последовательные реакции транспорта глюкозы в клетку. В результате происходящих каскадных механизмов запускается транспорт глюкозы в клетку, опосредованный инсулином. Важная роль в формировании инсулинорезистентности отводится генетически детерминированному нарушению тирозинкиназного пути фосфорилирования инсулинового рецептора. Серинфосфорилирование рецептора ингибирует активность тирозинкиназы инсулинового рецептора. У пациенток с СПКЯ доказано ингибирование трансдукции инсулинового сигнала в клетку в результате превалирования серинфосфорилирования. Те же механизмы усиливают активность цитохрома Р450с17 — ключевого в синтезе андрогенов как в яичниках, так и в надпочечниках.
Определённая роль в периферической инсулинорезистентности принадлежит гиперандрогении, поскольку андрогены изменяют структуру мышечной ткани в сторону превалирования мышечных волокон II типа, менее чувствительных к инсулину. Сопутствующее ожирение, чаще висцеральное, примерно у 50% пациенток усугубляет имеющиеся нарушения чувствительности к инсулину, оказывая синергичный эффект.
В норме не инсулин, а больше инсулиноподобный фактор ростаI играет важную роль в стероидогенезе. Но действие инсулина в концентрации выше нормы реализуется не только через инсулиновые рецепторы, но и рецепторы инсулиноподобного фактора ростаI. Инсулин и инсулиноподобный фактор ростаI способствуют усилению ЛГзависимого синтеза андрогенов в текаклетках и строме, стимулируют избыточную секрецию ЛГ. Инсулин также повышает активность цитохрома Р450с17, таким образом увеличивая продукцию овариальных и адренальных андрогенов. Гиперандрогении также способствует увеличение концентрации свободного биологически активного тестостерона изза уменьшения образования ГСПГ в печени. Показано, что инсулин регулирует продукцию ГСПГ. При гиперинсулинемии синтез ГСПГ снижается, что приводит к повышению концентраций свободных фракций как тестостерона, так и эстрадиола. Кроме того, инсулин подавляет продукцию белков, связывающих инсулиноподобный фактор ростаI, повышая их биологическую активность, а следовательно, синтез андрогенов в яичниках.
Роль ожирения сводится к внегонадному синтезу тестостерона и эстрона. Этот процесс имеет автономный характер, не зависит от гонадотропной стимуляции. Эстрон, синтезирующийся в жировой ткани, замыкает «порочный круг» в патогенезе формирования ПКЯ, повышая чувствительность гипофиза к ГнРГ.
Овариальные факторы. Последние исследования объясняют гиперпродукцию андрогенов генетически обусловленной дисрегуляцией цитохрома Р450с17 — ключевого фермента в синтезе андрогенов в яичниках и надпочечниках. Активность данного цитохрома регулируют те же механизмы, что участвуют в активации инсулинового рецептора, т.е. имеет место генетическая детерминанта овариальной, надпочечниковой гиперандрогении и инсулинорезистентности. Показано, что у пациенток с СПКЯ в крови повышена концентрация ингибитора апоптоза, т.е. снижается процесс атрезии фолликулов, которые персистируют.
Известно, что примерно у 50% пациенток с СПКЯ отмечают надпочечниковую гиперандрогению. Механизмы повышенной продукции ДГЭАС при нормальной и избыточной массе тела различны. У пациенток с нормальной массой тела (примерно у 30%) имеет место генетически обусловленная дисрегуляции цитохрома Р450с17, что приводит к повышенной продукции адренальных и овариальных андрогенов по единому механизму. У пациенток с ожирением активация андрогенной функции надпочечников обусловлена избыточной продукцией кортиколиберина и, соответственно, АКТГ, поэтому увеличивается синтез не только ДГЭАС, но и кортизола.
На основании анализа результатов многочисленных исследований можно предложить два варианта патогенеза СПКЯ у пациенток с нормальной массой тела и у инсулинорезистентных пациенток (рис. 181, 182). На генетические причины надпочечниковой и яичниковой гиперандрогении у пациенток с нормальной массой тела указывают и данные анамнеза и клинической картины, поскольку частота перенесённых заболеваний не выше, чем в популяции, и, кроме как нарушений менструальной и генеративной функции, пациенток ничего не беспокоит. Тогда как у пациенток с ожирением повышена частота ОРВИ и много диэнцефальных симптомов, что указывает на центральный, гипоталамический генез формирования СПКЯ — нарушение нейроэндокринного контроля секреции ГнРГ.
Патогенез СПКЯ у инсулинорезистентных больных представляется следующим образом (рис. 18-2). Пубертатный период характеризуется инсулинорезистентностью изза повышенной продукции гормона роста. Инсулин — важный митогенный гормон, необходим в пубертатном периоде в повышенных концентрациях для нормального физического развития и созревания органов и тканей репродуктивной системы. Как уже отмечалось, это критический период в жизни, когда может быть манифестация любой генетически обусловленной патологии, особенно под воздействием различных средовых факторов.
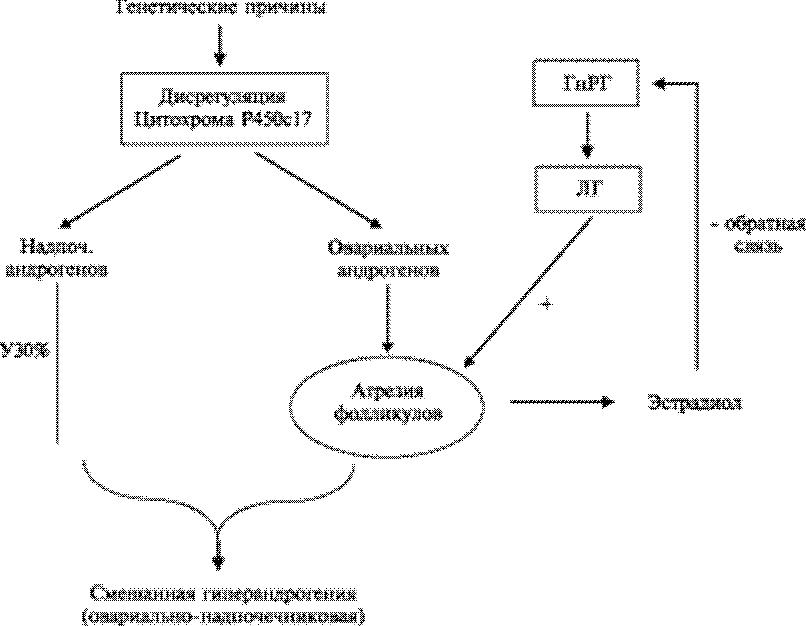
Рис. 18-1. Патогенез СПКЯ у пациенток с нормальной массой тела.
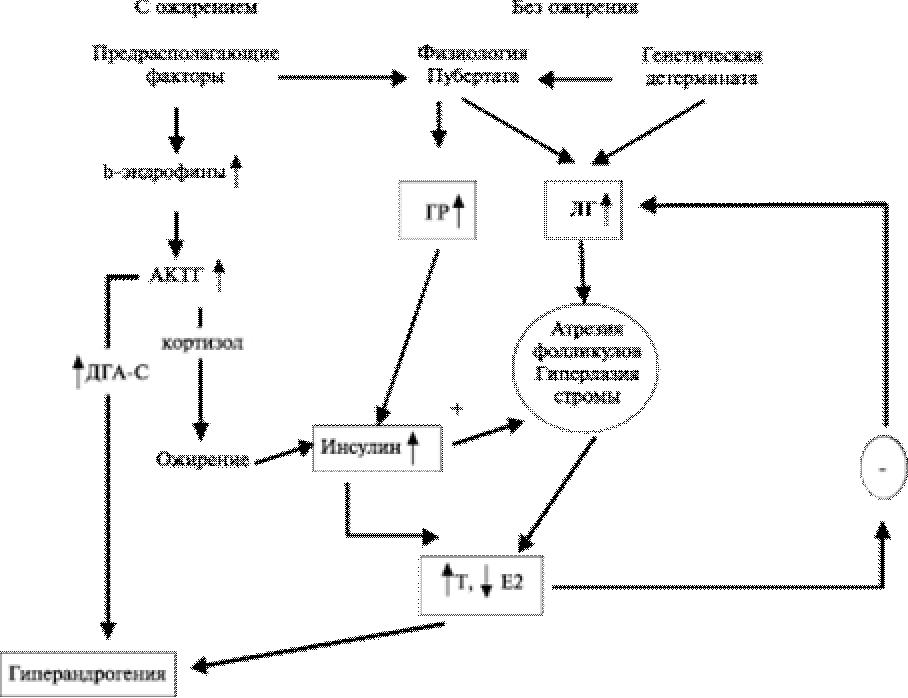
Рис.18-2. Патогенез СПКЯ у инсулинорезистентных больных.
Таким образом, патогенез СПКЯ многофакторный, с вовлечением в патологический процесс овариальных, надпочечниковых и экстраовариальных факторов и имеет различные механизмы у пациенток с нормальной массой тела, ожирением, инсулинорезистентностью.
КЛИНИЧЕСКАЯ КАРТИНА СИНДРОМА ПОЛИКИСТОЗНЫХ ЯИЧНИКОВ
Клиническая картина СПКЯ характеризуется нарушением менструального цикла, первичным бесплодием, избыточным оволосением, угревой сыпью. В последние годы всё чаще (около 50%) встречаются женщины с нормальной массой тела, слабовыраженными андрогензависимыми дерматопатиями, так называемые безгирсутные пациентки. Менархе своевременный — 12–13 лет. Нарушение менструального цикла с периода менархе — по типу олигоменореи у подавляющего большинства женщин (70%), реже дисфункциональные маточные кровотечения (7–9%). Вторичная аменорея (до 30%) встречается у нелеченых женщин старше 30 лет при сопутствующем ожирении, а у пациенток с нормальной массой тела наблюдается с менархе и не зависит от длительности ановуляции.
ДИАГНОСТИКА СИНДРОМА ПОЛИКИСТОЗНЫХ ЯИЧНИКОВ
В настоящее время большинство исследователей приняли критерии диагностики, предложенные на Роттердамском консенсусе в 2004 г.: олигоменорея и/или ановуляция, гиперандрогения (клинические и/или биохимические проявления), эхографические признаки поликистозных яичников. Наличие двух из трёх этих признаков диагностирует СПКЯ при исключении других причин формирования ПКЯ.
АНАМНЕЗ
В анамнезе у пациенток с нормальной массой тела частота перенесённых заболеваний не выше, чем в популяции; при ожирении — большая частота перенесённых нейроинфекций, экстрагенитальной патологии, отягощённая наследственность по инсулинонезависимому сахарному диабету, ожирению, артериальной гипертонии.
ФИЗИКАЛЬНОЕ ИССЛЕДОВАНИЕ
При физикальном исследовании морфотип женский, при избыточной массе тела у большинства пациенток висцеральный тип распределения жировой ткани; степень выраженности гирсутизма от скудного до выраженного. Определяют индекс массы тела: избыточной масса тела считается при индексе массы тела более 26 кг/м2, а ожирение — при индексе массы тела свыше 30 кг/м2. В зависимости от характера распределения жировой ткани ожирение может быть по женскому типу, или гиноидное (равномерное распределение жировой ткани), или по мужскому типу (центральное, кушингоидное, андроидное, висцеральное) с преимущественным отложением жировой ткани в области плечевого пояса, передней стенки живота и мезентерии внутренних органов. Висцеральный тип ожирения чаще сопровождается инсулинорезистентностью и наблюдается у 80% пациенток с СПКЯ и избыточной массой тела. Рекомендуют определять не только индекс массы тела, но и отношение объёма талии к объёму бёдер. Этот индекс характеризует тип ожирения и риск возникновения метаболических нарушений. Отношение объёма талии к объёму бёдер более 0,85 соответствует висцеральному типу, а менее 0,85 — женскому типу ожирения.
Клиническим проявлением инсулинорезистентности считается наличие «нигроидного акантоза»: участки гиперпигментации кожи в местах трения (паховая, подмышечная области и др.). При пальпации молочных желёз у большинства пациенток определяют признаки фибрознокистозной мастопатии. При гинекологическом исследовании у пациенток с нормальной массой тела определяют увеличенные яичники.
ЛАБОРАТОРНЫЕ ИССЛЕДОВАНИЯ
При исследовании уровня гормонов в крови у большинства пациенток определяют повышенную концентрацию ЛГ, тестостерона, 17-ОП, увеличение соотношения ЛГ/ФСГ более 2,5; в 50–55% наблюдений — снижение концентрации ГСПГ, повышение концентрации ДГЭАС, у 25% пациенток — повышение концентрации пролактина. Чувствительный метод диагностики гиперандрогении — определение индекса свободных андрогенов, который рассчитывается по следующей формуле:
Индекс свободных андрогенов = Общ.Т x 100 / ГСПГ
Значительное повышение уровней 17-ОП и ДГЭАС требует исключения в первую очередь ВГКН. Для этого в современной клинической практике используют пробу с АКТГ. Повышение уровня 17ОП и ДГЭАС (более чем в 8–10 раз) в ответ на введение АКТГ свидетельствует о ВГКН, причиной которой является генетически детерминированный дефицит фермента 21гидроксилазы.
Участие яичников и надпочечников в синтезе тестостерона примерно одинаково — по 30%. Поэтому повышенная концентрация тестостерона не может дифференцировать надпочечниковую и яичниковую гиперандрогению. В связи с чем, практикующим врачам с целью дифференциальной диагностики можно рекомендовать определение в плазме крови ДГЭАС — основного маркёра надпочечниковой гиперандрогении, до и после пробы с дексаметазоном. Исследование 17кортикостероидов и стероидного профиля мочи малоинформативно, поскольку отражает метаболизм всех андрогенов и не может точно выявить их источник даже после проведения пробы с дексаметазоном.
Диагностика метаболических нарушений в первую очередь направлена на выявление инсулинорезистентности методом орального глюкозотолерантного теста. При этом в крови определяют базальный и стимулированный приёмом 75 г глюкозы уровень инсулина и глюкозы. Если через 2 ч уровень глюкозы крови приходит к исходным цифрам, а инсулина — нет, это свидетельствует об инсулинорезистентности. Если через 2 ч повышен уровень не только инсулина, но и глюкозы, это свидетельствует о нарушенной толерантности к глюкозе. При этом отмечается повышение базальной концентрации инсулина. На следующем этапе метаболических нарушений развивается инсулинонезависимый сахарный диабет, который диагностируют при повышенной базальной концентрации и глюкозы, и инсулина. При этом проведение глюкозотолерантного теста не рекомендуют.
Основные клинические и биохимические критерии инсулинорезистентности: висцеральное ожирение, «нигроидный акантоз», стимулированная глюкозой гиперинсулинемия, уровень инсулина натощак 12,2 мМЕ/л и более, индекс HOMA более 2,5 (инсулин натощак x глюкоза натощак / 22,5).
ИНСТРУМЕНТАЛЬНЫЕ ИССЛЕДОВАНИЯ
Важнейший метод в диагностике СПКЯ эхоскопическая картина поликистозных яичников.
Эхоскопические критерии поликистозных яичников:
- объём яичников более 8 см3;
- увеличение площади гиперэхогенной стромы;
- число анэхогенных фолликулов диаметром до 10 мм не менее десяти;
- усиленный кровоток и обильная сосудистая сеть в строме (при доплерометрии).
В отличие от эхоскопической картины мультифолликулярных яичников, характерных для раннего пубертата, гипогонадотропной аменореи, синдрома резистентных яичников, специфическим проявлением мультифолликулярных яичников при УЗИ является небольшое число фолликулов диаметром около 10 мм, расположенных по всему яичнику между небольшим количеством стромы со слабым эхосигналом, причём объём яичников не превышает 8 см3.
По данным эхографического и эндоскопического обследований, выделено два типа поликистозных яичников в зависимости от расположения фолликулов по отношению к строме: I тип поликистозных яичников — диффузное — и II тип — периферическое расположение фолликулов по отношению к гиперэхогенной строме. I тип чаще наблюдают у пациенток с нормальной массой тела, скудным гирсутизмом, резистентных к кломифену, большой частотой вторичной аменореи и СГЯ. II тип поликистозных яичников (классический), всем хорошо известный, чаще выявляют у больных с ожирением. Именно у пациенток с I типом поликистозных яичников в анамнезе имелись беременности, закончившиеся самопроизвольным прерыванием в ранних сроках. По тестам функциональной диагностики у них периодически тестируются овуляторные циклы с НЛФ, при этом визуальный осмотр при лапароскопии выявляет текалютеиновые кисты диаметром 10–20 мм по типу синдрома лютеинизации неовулированного фолликула. При этом яичники больших размеров, капсула яичника тонкая, но гладкая без стигм, что свидетельствует об ановуляции. Данный клиникоморфологический вариант СПКЯ (нормальная масса тела, скудный гирсутизм, большая частота вторичной аменореи, I тип поликистозных яичников) встречается всё чаще. Среди этих пациенток наблюдают «овулирующие поликистозные яичники» (примерно у 9–11%). Нередко при лапароскопии выявляют СГЯ без предшествующего применения стимуляторов овуляции в виде текалютеиновых кист, иногда многокамерных, общим размеров от 5 до 10 см в диаметре. Это так называемая эндогенная гиперстимуляция за счёт влияния собственных гонадотропинов, уровень которых может быть нормальным, встречается примерно у 11–14% пациенток с I типом поликистозных яичников. Данный факт свидетельствует о гиперреакции текаклеток на нормальную концентрацию ЛГ.
Биопсия эндометрия показана женщинам с ациклическими кровотечениями в связи с большой распространённостью гиперпластических процессов эндометрия. В настоящее время не вызывает сомнений, что у женщин с СПКЯ высокий риск развития рака эндометрия. К отягощающим факторам относятся метаболические нарушения и длительность ановуляции.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА СИНДРОМА ПОЛИКИСТОЗНЫХ ЯИЧНИКОВ
Дифференциальную диагностику проводят у пациенток с нормальной массой тела с ВГКН, а при ожирении — с вторичными поликистозными яичниками у пациенток с метаболическим синдромом (табл. 18-1, 18-2). Как видно из представленных данных, при формировании вторичных поликистозных яичников гормональная и эхографическая картина не отличается от таковой при СПКЯ с ожирением. Только на основании данных анамнеза (наличие периода регулярных менструаций, беременностей, родов, вторичное нарушение менструальной и генеративной функции на фоне прибавки массы тела) можно отличить СПКЯ с ожирением от вторичных поликистозных яичников. На наш взгляд, это важно для практикующих врачей, поскольку длительность хронической гиперандрогенной ановуляции будет значительно выше у пациенток с СПКЯ (с менархе) и ожирением, что, в первую очередь, будет отражаться на эффективности различных методов стимуляции овуляции.
Таблица 18-1. Дифференциально-диагностические критерии ВДКН и СПКЯ при нормальной массе тела
| Показатель | ВГКН | СПКЯ (синдром поликистозных яичников) |
| Морфотип | Интерсексуальный | Женский |
| Гирсутизм | II–III степени | Скудный — I степени |
| Менструальный цикл | Неустойчивый, реже «нестойкая» олигоменорея | Олигоаменорея с менархе |
| Генеративная функция | Невынашивание — 90%Бесплодие — 10% | Бесплодие I — 90% |
| ТФД | НЛФ, периодически ановуляция | Ановуляция |
| ЛГ/ФСГ | <1,5 | >2,5 — 70% |
| ДГЭАС | у 100% | у 30-35% |
| УЗИ | Норма или мультифолликулярные яичники | Чаще I тип поликистозных яичников |
Таблица 18-2. Дифференциально-диагностические критерии вторичных ПКЯ на фоне МС и СПКЯ с ожирением
| Показатель | НОЭС (нейрообменно-эндокринный синдром) | Показатель НОЭС (нейрообменно-эндокринный СПКЯ (синдром поликистозных яичников) |
| Морфотип | «Кушингоидный» | «Кушингоидный» у 80% |
| Гирсутизм | Вторично на фоне прибавки массы тела | С менархе |
| Нарушение менструальной функции | Вторично на фоне прибавки массы тела | С менархе |
| Генеративная функция | Бесплодие II — 80% | Бесплодие I — 90% |
ЛЕЧЕНИЕ СИНДРОМА ПОЛИКИСТОЗНЫХ ЯИЧНИКОВ
ЦЕЛИ ЛЕЧЕНИЯ
Лечение пациенток с СПКЯ направлено на:
- нормализацию массы тела и метаболических нарушений;
- восстановление овуляторных менструальных циклов;
- восстановление генеративной функции;
- устранение гиперпластических процессов эндометрия;
- устранение клинических проявлений гиперандрогении — гирсутизма, угревой сыпи.
МЕДИКАМЕНТОЗНОЕ ЛЕЧЕНИЕ СИНДРОМА ПОЛИКИСТОЗНЫХ ЯИЧНИКОВ
Независимо от конечной цели лечения на первом этапе необходима нормализация массы тела и коррекция метаболических нарушений. Комплексная метаболическая терапия, включающая принципы рационального питания и медикаментозные средства, подробно изложена в разделе «Метаболический синдром».
У инсулинорезистентных пациенток с нормальной массой тела рекомендуют на I этапе терапию метформином — препаратов из класса бигуанидов. Метформин приводит к снижению периферической инсулинорезистентности, улучшая утилизацию глюкозы в печени, мышцах и жировой ткани. Препарат назначают по 1000–1500 мг в сутки под контролем глюкозотолерантного теста. Длительность терапии 3–6 мес, в том числе на фоне стимуляции овуляции.
Стимуляцию овуляции проводят у пациенток, планирующих беременность, после нормализации метаболических нарушений. На первом этапе индукции овуляции применяют кломифена цитрат. Надо отметить, что длительно применявшийся метод стимуляции овуляции назначением эстрогенгестагенных препаратов, основанный на ребаунд- эффекте после их отмены, не потерял своей популярности. Кломифена цитрат относится к синтетическим антиэстрогенам — классу селективных модуляторов ЭР. Механизм его действия основан на блокаде ЭР на всех уровнях репродуктивной системы. После отмены кломифена цитрата по механизму обратной связи происходит усиление секреции гонадолиберина, что нормализует выброс ЛГ и ФСГ и, соответственно, овариальный фолликулогенез. Кломифена цитрат назначают с 5-го по 9-й день менструального цикла по 50–100 мг в день. Если нет эффекта при назначении 100 мг, то дальнейшее увеличение дозы кломифена цитрата нецелесообразно. При отсутствии овуляции при максимальной дозе в течение 3 месяцев пациентку можно считать резистентной к кломифена цитрату. Критерием оценки эффективности проводимой стимуляции овуляции служит восстановление регулярных менструальных циклов с гипертермической базальной температурой в течение 12–14 дней, уровень прогестерона в середине второй фазы цикла 15 нг/мл и более, а также подтверждение овуляции индивидуальным тестом, определяющим преовуляторный пик ЛГ в моче.
Гиперинсулинемия снижает эффективность стимуляции овуляции, поэтому инсулинорезистентным пациенткам с СПКЯ кломифена цитрат назначают на фоне приёма метформина, что повышает частоту наступления овуляции и беременности по сравнению с монотерапией кломифена цитратом. Длительность гиперандрогенной ановуляции (более 10 лет), возраст старше 28 лет также могут способствовать резистентности к кломифена цитрату. Можно выделить следующие критерии кломифенрезистентности: возраст старше 30 лет, индекс массы тела >25, объём яичников >10 см3, уровень ЛГ >15 МЕ/л, уровень эстрадиола <150 пмоль/л.
Комбинированные схемы лечения кломифена цитратом. Назначение овуляторной дозы 10000 МЕ ХГЧ может увеличить вероятность наступления беременности при отсутствии реакции только на кломифена цитрат. При этом необходим ультразвуковой мониторинг растущего фолликула, ХГЧ вводят при диаметре доминантного фолликула не менее 18 мм, после чего овуляция отмечается через 34–36 ч. Ультразвуковой мониторинг проводят также с целью оценки состояния эндометрия, толщина которого должна быть не менее 6 мм, иначе нарушается процесс имплантации. В связи с антиэстрогенным эффектом кломифена цитрата может быть недостаточное натяжение цервикальной слизи в преовуляторном периоде, снижение пролиферативных процессов в эндометрии. Поэтому эффект кломифена цитрата в отношении индукции овуляции выше, чем в наступлении беременности. С целью лечения этих нежелательных эффектов рекомендуют назначение натуральных эстрогенов — эстрадиол в дозе 2–4 мг с 9-го по 14-й день цикла. При НЛФ можно увеличить дозу кломифена цитрата или назначить гестагены во вторую фазу цикла с 16-го по 25-й день. При этом предпочтительнее препараты натурального прогестерона (дидрогестерон 20 мг в сутки или прогестерон 200 мг в сутки).
Комбинированная терапия кломифена цитратом и гонадотропинами более эффективна. Кломифена цитрат назначают по 100 мг с 2–3-го по 6–7-й день цикла, далее — на 5-й, 7-й, 9-й, 11-й, 13й день вводят рекомбинантный ФСГ по 50–150 МЕ в сутки под ультразвуковым контролем фолликулогенеза. При диаметре преовуляторного фолликула не менее 18 мм вводят 10000 МЕ ХГЧ. Вторую фазу можно поддержать назначением гестагенов (дидрогестерон, прогестерон). При отсутствии беременности на фоне овуляторных циклов показана лапароскопия для исключения перитонеальных факторов бесплодия. В последние годы используют антагонисты ГнРГ с целью получения ребаундэффекта после их отмены (по аналогии с эстрогенгестагенными препаратами). Но на фоне антагонистов ГнРГ происходит более выраженное подавление гонадотропной функции, поэтому и эффект в стимуляции овуляции после отмены выше, чем после эстрогенгестагенных препаратов. Рекомендуют 4–6 инъекции антагонистов ГнРГ. Данный метод стимуляции овуляции предпочтительнее рекомендовать у молодых пациенток с нормальной массой тела при I типе поликистозных яичников во избежание развития СГЯ.
На втором этапе стимуляции овуляции у кломифенрезистентных пациенток с СПКЯ, планирующих беременность, назначают гонадотропины. Препараты последнего поколения созданы принципиально новыми технологиями. Одним из первых был рекомбинантный препарат чистого ФСГ — пурегон ©, его аналог — гоналФ ©, при применении которых меньше риск развития СГЯ. При назначении гонадотропинов пациентку нужно информировать о риске многоплодной беременности, возможном развитии СГЯ, а также о высокой стоимости лечения. В связи с этим лечение следует проводить только после исключения патологии матки и труб, мужского фактора бесплодия. Существует множество схем лечения гонадотропинами (подробно они описаны в соответствующих руководствах). Основной принцип лечения гонадотропинами — строгий трансвагинальный ультразвуковой мониторинг для своевременного прекращения стимуляции с целью предотвращения развития СГЯ. Применение антагонистов ГнРГ в протоколах стимуляции овуляции у пациенток с СПКЯ находит всё более широкое применение, поскольку подавляет пики избыточной секреции ЛГ, что улучшает качество овоцитов и снижает риск развития СГЯ.
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ СИНДРОМА ПОЛИКИСТОЗНЫХ ЯИЧНИКОВ
Хирургический метод стимуляции овуляции лапароскопическим доступом наиболее популярен у кломифенрезистентных женщин с СПКЯ в связи с доступной стоимостью лечения. Кроме того, к преимуществам лапароскопии относится отсутствие риска СГЯ, наступления многоплодной беременности и возможность ликвидации часто сопутствующего перитонеального фактора бесплодия. Помимо клиновидной резекции, при лапароскопии предложена каутеризация яичников при помощи различных энергий (термо, электро, лазерной), которая основана на разрушении стромы. Отсутствие овуляции в течение 2–3 циклов требует дополнительного назначения кломифена цитрата, а у инсулинорезистентных пациенток — метформина, что повышает частоту наступления беременности. Как правило, беременность наступает в течение 6–12 мес, в дальнейшем частота наступления беременности уменьшается.
Выбор методики хирургической стимуляции овуляции зависит от типа и объёма поликистозных яичников, длительности ановуляции. При значительном увеличении объёма поликистозных яичников независимо от типа рекомендуют клиновидную резекцию. При незначительном увеличении объёма поликистозных яичников можно проводить эндокоагуляцию стромы по типу демедуляции. Такая тактика основана на патогенетических механизмах хирургической стимуляции овуляции — проводят максимальное удаление (или разрушение) андрогенсекретирующей стромы поликистозных яичников, в результате уменьшается внегонадный синтез эстрона из тестостерона, нормализуется чувствительность гипофиза к гонадолиберину.
ДАЛЬНЕЙШЕЕ ВЕДЕНИЕ
Несмотря на достаточно высокую суммарную эффективность различных методов стимуляции овуляции (75–80%) в восстановлении овуляции и фертильности у пациенток СПКЯ, большинство практикующих врачей отмечают рецидив симптоматики. В основном рецидив наблюдают у пациенток, которые реализовали генеративную функцию при использовании консервативных методов лечения, а также после каутеризации поликистозных яичников. Поэтому после родов необходима профилактика рецидива СПКЯ, как и риска развития гиперпластических процессов эндометрия и отдалённых последствий инсулинорезистентности — сердечнососудистые заболевания, инсулинонезависимый сахарный диабет. С этой целью наиболее целесообразно назначение КОК, предпочтительнее монофазных (ярина ©, жанин ©, марвелон ©, диане © и др.), а у пациенток с ожирением рекомендовано введение интравагинальной гормональной рилизинговой системы НоваРинг ©, при использовании которой нет прибавки массы тела. При плохой переносимости КОК можно рекомендовать гестагены во второй фазе цикла.
Лечение гиперпластических процессов эндометрия. При выявлении гиперплазии эндометрия, подтверждённой гистологическим исследованием, на первом этапе проводят терапию эстрогенгестагенами, прогестагенами или антагонистами ГнРГ, при ожирении предпочтительнее прогестагены. Гормонотерапия гиперпластических процессов эндометрия предусматривает центральный и местный механизм действия препарата, заключающийся в подавлении гонадотропной функции гипофиза, что тормозит фолликулогенез и, как следствие этого, снижает эндогенный синтез стероидов; местное действие гормональных препаратов способствует атрофическим процессам эндометрия. Гормональное лечение гиперплазии эндометрия у инсулинорезистентных пациенток с СПКЯ проводят на фоне метаболической терапии. Без коррекции метаболических нарушений (гиперинсулинемии, гипергликемии, дислипидемии) закономерен рецидив, что связано с ролью жировой ткани в стероидогенезе, а также гиперинсулинемии в усугублении имеющихся эндокринных нарушений при СПКЯ.
Для регуляции менструального цикла и лечения андрогензависимых дерматопатий рекомендуют КОК с антиандрогенным действием. Пролонгированный режим приёма КОК более эффективен в редукции гирсутизма, поскольку в семидневный перерыв восстанавливается гонадотропная функция гипофиза, а следовательно, и синтез андрогенов.
СПИСОК ЛИТЕРАТУРЫ
Геворкян М.А., Манухин И.Б. и соавт. // Проблемы репродукции. — 2004. — № 3. — С. 20.
Манухин И.Б., Геворкян М.А., Кушлинский Н.Е. // Акушерство и гинекология. — 2001. —№ 6. — С. 33–36.
Манухин И.Б., Геворкян М.А., Кушлинский Н.Е. Синдром поликистозных яичников. — М., 2004. — 240 с.
Манухин И.Б., Тумилович Л.Г., Геворкян М.А. Клинические лекции по гинекологической эндокринологии. — М., 2006.
Назаренко Т.А. Синдром поликистозных яичников. — М., 2005. — С. 100–138.
Azziz R., Bradley E.L., Potter H.D., Boots L.R. // J. Clin. Endocrinol. Metab. — 1995. — Vol. 80. — P. 400–405.
Bachmann G.A. // Am. J. Obstet. Gynecol. — 1998. — Vol. 179, N 6. — P. S87–89.
Barnes R.B. // J. Endocrinol. Invest. — 1998. — Vol. 21. — P. 567–579.
Ciampelli M., Guido M. et al. // Fertil. Steril. — 2000. — Vol. 73, N 4. — P. 712–716.
De Leo V., Ia Marca A., Orvieto R. et al. // J. Clin Endocrinol Metab. — 2000. — Vol. 85. — P. 1598–1600.
Kelstimur F., Sahin Y. // Fertil Steril. — 1998. — Vol. 69. — P. 66–69.
Kolodziejczyk B., Duleba A.J. et al. // Fert. Steril. — 2000. — Vol. 73, N 6. — P. 1149–1154.
Rosenfield R. In bock Polycystic ovary syndrome. — 2001. — P. 51–61.
Tsilchorozidou T., Overton C., Conway G. // Clin. Endocrinol (Oxf). — 2004. — Vol. 60. — P. 1–17.
Источник: Гинекология - национальное руководство под ред. В.И. Кулакова, Г.М. Савельевой, И.Б. Манухина 2009 г.

